Rýchlosť chemických reakcií
Vzdelávacia oblasť: PREMENY LÁTOK
Tematický celok: ZMENY PRI CHEMICKÝCH REAKCIÁCH
Téma: RÝCHLOSŤ CHEMICKEJ REAKCIE
Je reakcia pomalá či rýchla?
Predstavu o rýchlosti chemickej reakcie získame pozorovaním jej priebehu! Pozorujeme/všímame si ako rýchlo vzniká produkt, ako rýchlo sa míňa reaktant, ako rýchlo sa reaktant mení na produkt, ako rýchlo sa mení sfarbenie, skupenstvo, vzhľad reagujúcich látok.
Čo je to rýchlosť chemickej reakcie?
Čas potrebný na zmenu reaktantov na produkty.
Pozorne si pozri videoprezentáciu:
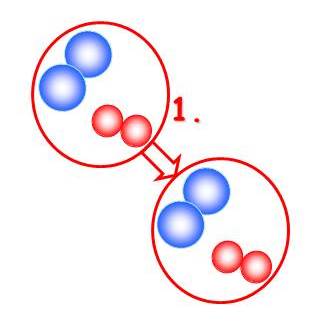
Nasledujúca animácia predstavuje reakčnú zmes. Modré a červené guličky znázorňujú molekuly dvoch rôznych chemických látok, ktoré sú reaktantami v chemickej reakcii. Aby k chemickej reakcii došlo a vznikla nová chemická látka, teda produkt, reaktanty sa musia k sebe dostať a „zraziť sa“.
1. ANIMÁCIA:
Keďže molekuly reaktantov nie sú k sebe vhodne orientované, správne natočené, ich zrážka nespôsobí chemickú reakciu a nevznikne nový produkt.
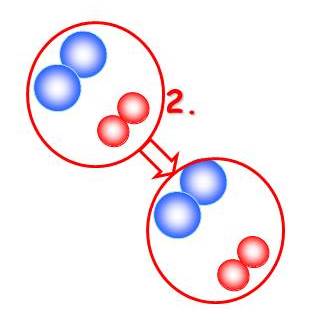
2. ANIMÁCIA:
Hoci molekuly reaktantov sú vhodne orientované, správne natočené k sebe, nemajú dosť energie, sily na to, aby spolu zreagovali a vytvorili novú látku.
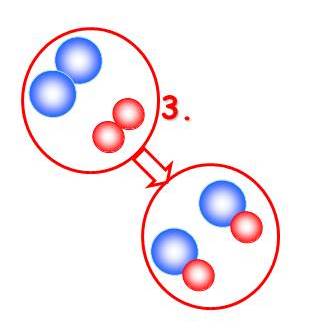
3. ANIMÁCIA:
Reaktanty, správne k sebe otočené, vhodne orientované a s dostatočnou energiou úspešne zreagujú a vzniká nová chemická látka – produkt.
Pokús sa zodpovedať nasledovné otázky:
1. Akým spôsobom zistíš, či je chemická reakcia pomalá alebo rýchla?
2. Čo konkrétne pozoruješ, keď pozoruješ rýchlosť chemickej reakcie?
3. Čo je to rýchlosť chemickej reakcie?
4. Vymenuj pomalé a rýchle chemické reakcie.
5. Pôsobenie kyslých dažďov je pomalá chemická reakcia. Na čo všetko pôsobia a ako?
6. Ako sa rieši problém pomalého rozkladu plastov?
7. V ktorom prípade je plesnivenie potravín žiaduce?
8. Chemické reakcie v ľudskom tele sú relatívne rýchle. Zamysli sa a vysvetli prečo?
9. Akým spôsobom spomalíš kazenie potravín?
10. Veľkým problémom kovových konštrukcií je hrdzavenie. Môžeme hrdzavenie nejakým spôsobom spomaliť?
11. Kde sa využíva urýchľovanie chemických reakcií?
12. Čo sa musí stať s reaktantami, aby došlo k chemickej reakcii?
13. Kedy sa stáva zrážka medzi reaktantami úspešnou?
14. Vysvetli, čo to znamená, že častice sú vhodne orientované.
15. Prečo je dôležité, aby častice mali dostatok sily pri chemickej zrážke?
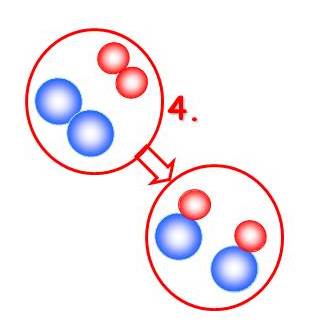
16. Pozri so obrázky vyššie (č.1 až 4) a urči, v ktorom prípade bola zrážka úspešná a k v ktorom nie. Svoje tvrdenie zdôvodni.
17. Porozmýšľaj, akým spôsobom by si mohol(a) dodať energiu reaktantom, aby mali dostatok sily k úspešnej zrážke a chemickej reakcii?
18. Porozmýšľaj, ako by si docielil(a), aby čím najviac častíc v reakčnej zmesi bolo správne k sebe otočených/orientovaných a tak sa stala ich zrážka úspešnou?