Redukcia striebra a rad reaktivity kovov
Vzdelávacia oblasť: VÝZNAMNÉ CHEMICKÉ PRVKY A ZLÚČENINY
Tematický celok: NEUTRALIZAČNÉ A REDOXNÉ REAKCIE
Téma: REDOXNÉ DEJE
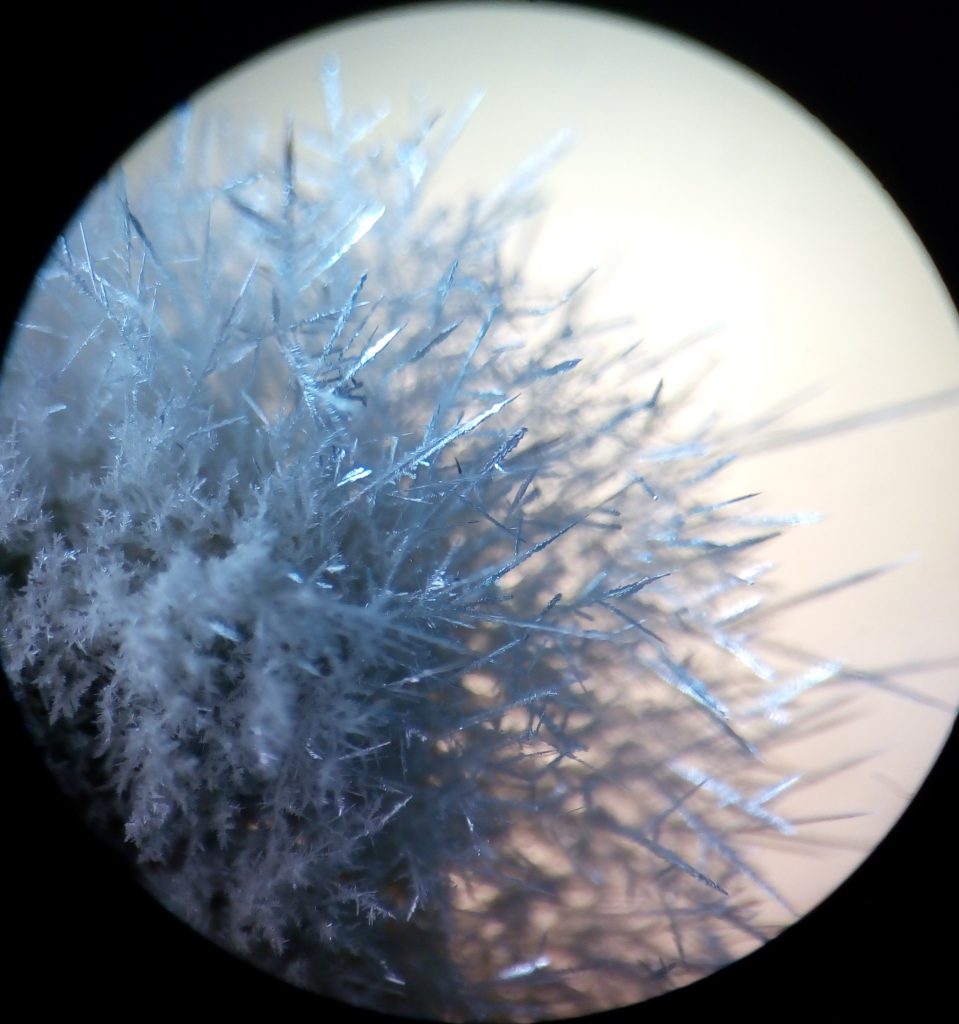
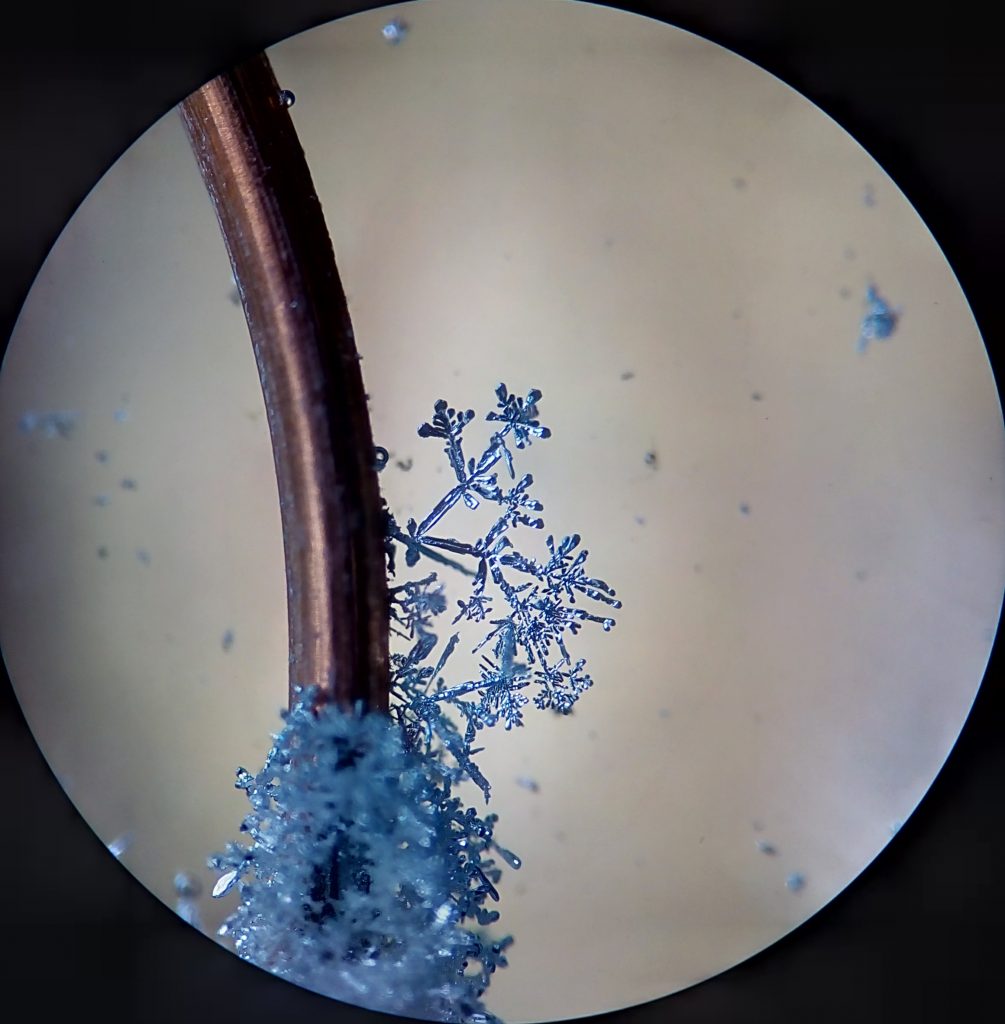
Pamätáš si na experiment z chémie, v ktorom sme dokázali pripraviť kryštáliky čistého striebra?
Chemický dej prebieha podľa nasledovnej chemickej reakcie:
Cu + AgNO3 -> Cu(NO3)2 + Ag
Tento experiment si nemôžeš vyskúšať doma, preto si pozri video alebo fotografie z nášho chemického krúžku Kremík na pripomenutie.
Vysvetlenie, prečo medený drôtik reaguje s katiónom striebra, nájdeš v Elektrochemickom rade napätia kovov (Rad reaktivity kovov).
Pokús sa odpovedať na otázky:
1. Chemickú reakciu vyrovnaj na chemickú rovnicu.
2. Doplň oxidačné čísla všetkých prvkov.
3. O aký typ reakcie sa jedná?
4. Napíš čiastkové deje oxidácie a redukcie.
5. Doplň názvy chemických látok: Cu, AgNO3, Cu(NO3)2, Ag
6. Porozmýšľaj, čo spôsobilo zmenu farby bezfarebnej kvapaliny na modrú po prebehnutí reakcie?
7. Latinský názov striebra je ARGENTUM. Vyhľadaj, čo tento názov znamená, z akého slova pochádza.
8. Striebro patrí medzi ušľachtilé kovy. Aké všeobecné vlastnosti ušľachtilé kovy majú?
9. Pomocou Radu reaktivity kovov vysvetli, ako je možné, že na medenom drôtiku vyrastú kryštáliky striebra.
10. Bola by možná aj opačná reakcia – reagovalo by čisté striebro s katiónom medi? Vysvetli.
11. Vymysli vlastnú pomôcku (básničku, riekanku, slovnú hračku) na ľahšie zapamätanie si Radu reaktivity kovov.
12. Látkové množstvo dusičnanu meďnatého, ktorý vznikol vyššie uvedenou reakciou je 0,56mol. Aká je hmotnosť vzniknutého dusičnanu meďnatého?